有沒有人員對檢測限、定量限、報(bào)告限、忽略限及他們之間迷霧一般的關系有諸多困惑?在工作中、培訓中也有很多人問過老王,一些問題可能重複解答過多次。閑暇之時,老王把自己對於(yú)他們及他們之間的錯綜關系和應用要點進行梳理總結,今天與大家聊聊,或可供參考。
一、定義與釋義:
檢測限Detection Limit(限度試驗):試樣中被測物質被檢測出的最低量。從定義來看這一指标隻能用於(yú)限度檢查,而不能進行報(bào)告定量結果。
定量限Quantitation Limit(定量試驗):試樣中被測(cè)物質被定量測(cè)定的最低量,其測(cè)定結果應符合準確(què)度和精密度要求。(也是成線性範圍的最低濃度或量),可衡量方法靈敏度與定量檢測(cè)能力。
報(bào)告限(Reporting Threshold):高於(yú)此限度的降解産物需報(bào)告其含量。法規要求大於(yú)該限度必須報(bào)告的,是基於(yú)質量可控性的科學性和嚴格性的平衡。
忽略限Disregard Limit:字面理解,低於(yú)此限度的雜質可直接忽略不計,執行層面可理解爲低於(yú)此限度的單個雜質可不報(bào)告,可不計入雜質總和。
二、如何獲得檢測(cè)限、定量限、報(bào)告限?
定量限與檢測(cè)限是對於(yú)分析方法的檢出能力和靈敏度的測(cè)試,需經方法驗證而得。
1、檢測(cè)限:通常的做法是配制一個溶液,通過稀釋獲得信噪比≥3:1的溶液作爲定量限(日常爲瞭(le)方便稀釋與計算、以及看檢測(cè)限與定量限的對應關系,通常可先做定量限,然後用定量限溶液再稀釋爲檢測(cè)限)。
常見問題:方法驗證中,檢測(cè)限的信噪比大於(yú)10:1,是否還能将這個水平當做檢測(cè)限?
當然不能,既然信噪比已經大於(yú)10:1,也就說明可以準確定量瞭(le),爲什麽還要當做檢測限,可能會導緻一些雜質不被報告。
2、定量限:通常的做法是配制一個溶液,通過稀釋獲得信噪比≥10:1的溶液作爲定量限。也可直接用一定濃度的溶液直接進樣,信噪比>10:1即可。例如,報(bào)告阈值爲0.05%,則可直接使用≤0.05%對(duì)應的溶液進樣,查看信噪比符合即可。
3、做檢測(cè)限和定量限要點(diǎn)和注意事項
(1)選擇待測(cè)物質附近(前、後(hòu))基線平滑的基線,時間持續1min左右即可,但是需要注意6針中的同一成分的選擇時間應保持一緻(日常工作中可能部分不理解定量限考察意義的人員會選擇遠離待測(cè)成分的基線,選擇時段可能也不一樣的情況)
(2)一定要是連續進(jìn)樣,通常建議LOQ進(jìn)樣6針(因其要符合準確(què)度和精密度要求),LOD進(jìn)樣3針。
(3)LOQ信噪比6針(zhēn)均要≥10:1;LOD信噪比均要≥3:1
(4)ICH(Q3A、Q3B)中分析方法描述:定量限應不大於(yú)(≤)報告限”,故有關物質方法驗證/確(què)認中進行定量限試驗時,需要提前計算一下該藥品的日服用劑量,然後從ICH指導原則中看一下報告限是多少,驗證/確(què)認結果一定要與法規上的報告限進行對比,定量限不能大於(yú)報告限。
(5)如與CRO公司合作等,在接收、審核資料時也要注意。(常見問題,人員方法驗證作出的定量限大於(yú)ICH中的報(bào)告限)
(6)因檢測(cè)限、定量限除瞭(le)方法的靈敏與否之外,受儀器性能影響較大。做檢測(cè)限與定量限時,注意要考慮到不同性能、不同品牌儀器的差異,一定不能刻意去挑選性能和靈敏度非常好的儀器進行試驗。
(7)爲便於(yú)數據應用及撰寫資料方便,每針單獨計算信噪比(報(bào)告中需要報(bào)出);計算出定量限/檢測限濃度,如0.0502ug/ml,同時計算出定量限/檢測限(相當於(yú)供試品濃度的百分比)=定量限/檢測濃度/供試品濃度。
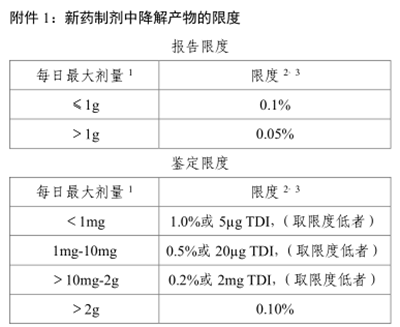
4、報(bào)告限:根據藥品的日服用劑量,詳見ICH指導(dǎo)原則(附圖1),其餘見“五、報(bào)告阈值
三、檢測限、定量限、報告限之間的關系是什麽?
ICH中規定定量限≤報(bào)告限,檢測限又小於(yú)定量限,從而推得3者的關系:檢測限<定量限≤報(bào)告限。
聊到這裏,可能有人著(zhe)急瞭(le),那他們和忽略限的關系呢?不要著(zhe)急,欲知關系如何,且聽下節分析。
四、聊聊“忽略限“?
說實話,這一節的标題老王想瞭(le)又想,覺得還是沒有合适的标題,隻能對”忽略限“先畫個問号,再逐步聊聊爲什麽。因爲忽略限這個名詞在EP或USP中會見到,中國藥典則會描述爲:“小於(yú)對照溶液XX倍的色譜峰忽略不計。”
USP在2022年01月份發瞭(le)一個關於(yú)“USP通則(zé)<621>色譜(pǔ)法-重要标準協調”的通告,其中有一條” 術語"可忽略限度(Disregard limit)"被"報告阈值(Reporting thresholds)"取代“的内容,計劃於(yú) 2022年12月1日起正式生效。此内容老王甚是贊同,因爲實際工作中有的叫做”忽略限“,有的叫做”報告限“,搞得分析人員一頭霧水,到底各自有什麽作用?互相有什麽關系?又有什麽不同?怎麽描述怎麽叫才合适呢?
其實,不論是叫做“忽略限“還是”報(bào)告限“,他們的目的是一樣的,叫做“忽略限”,那麽就是低於(yú)這個限度的雜質可以不報(bào)告,等於(yú)和高於(yú)這個限度的雜質需要報(bào)告;叫做“報(bào)告限”吧,等於(yú)或高於(yú)此限度的雜質就需要報(bào)告,低於(yú)此限度的雜質可不報(bào)告。
所以日常工作中,建議參考USP通則(zé)<621>色譜(pǔ)法中描述爲報(bào)告阈值(Reporting thresholds)較爲合适,就避免瞭(le)人員糾結到底是忽略限呢還是報(bào)告限呢……
五、如何建立每個(gè)品種的“報(bào)告阈值“呢?
USP還在2021年發瞭(le)一個關於“報告限”去留的内容,其中說瞭(le)FDA在多個藥品各論修訂意見中建議删除各論中的“報告限“,美國FDA認爲藥典各論無法對所有生産企業的每一個雜質或降解産物進行鑒定和羅列,那麽各論中設定“報告限”可能會導緻産品中某些高毒性雜質不被鑒定或報告。另外,美國FDA認爲每個藥物有其各自的特性,“報告限”應當因産品而異,企業應當在藥物申請時做出說明,美國FDA也會參考ICH的報告限作爲指導原則,對不同産品進行不同的考量。它是讓用戶基於藥物特性、最大攝入劑量等因素自主選擇“報告限”策略。USP則在接到美國FDA的意見後,開展瞭(le)一系列工作, 後續可能在修訂時删除已生效各論中的“報告限”,並(bìng)通過凡例的形式對“報告限”的選擇提供指導規範。
老王期待著(zhe)指導規範的發布,當然我也從質量控制與確保藥物的安全性角度考慮,建議大家建立各自産品”報告阈值“時,除瞭(le)考慮ICH中的報告限,基於藥物的安全性、如服用劑量等,雜質概況,還可考慮方法的靈敏度綜合制定。通常建議可用方法驗證得出的定量限作爲該産品的報告阈值,即能確保雜質結果準確定量,又不高於ICH中的報告限,而不建議直接用ICH中的報告限直接作爲報告阈值。
六、檢測(cè)限、定量限、報(bào)告阈值如何應用?
方法驗證完成後,可将檢測限(LOD)、定量限(LOQ)應用於(yú)後續的Sop編寫中,對分析人員合理報(bào)出檢驗結果具有指導意義。通常:
1、定量限的應用:
(1)可參(cān)考其制定”報(bào)告阈值“
(2)大於(yú)定量限的,即能夠準確(què)報出結果的直接報告數值即可。小於(yú)定量限的,可以報告小於(yú)定量限(<LOQ),同時可将LOQ備注出來。
結(jié)果報(bào)告示例:RRT約爲1.8的雜質<LOQ(0.03%)。
2、檢測限的應用:
(1)很多小夥伴對於(yú)積分參數的設置存有很多疑惑,那麽,如果你做瞭(le)檢測限,則可參考檢測限設置最小峰面積等制訂合理的積分參數,低於(yú)檢測限可不進行積分,避免過多的雜峰或基線波動幹擾;大於(yú)檢測限的色譜峰則積分、計算(積分、計算是爲瞭(le)分析雜質變化趨勢用)。
(2)可用於(yú)指導結果報告。如果檢測數據較小,小於(yú)檢測限,則可報告小於(yú)檢測限(<LOD)同時可将LOD備注出來。例如,RRT約爲0.8的雜質<LOD(0.01%);對於(yú)小於(yú)檢測限的情況也可報告爲未檢出,具體按照哪種方式報告,需要在各自管理文件中作出明確(què)規定。
3、報告阈值的應用:
前邊說瞭(le)爲瞭(le)分析各雜質的變化趨勢,對於(yú)大於(yú)檢測限的雜質要積分、計算,那麽是否需要報告呢?則需要視情況而定。若雜質含量超過可以報告的限度(如定量限、報告阈值)則可報告出單雜及可計入總雜質。
結語:以上爲個(gè)人理解與經(jīng)驗,如有不妥,敬請指正。
參考資料:
ICH Q2 分析方法驗(yàn)證(zhèng)
ICH Q3A 新原料藥(yào)中的雜(zá)質
ICH Q3B 新制劑(jì)中的雜(zá)質
USP關於(yú)“報(bào)告限”的去留(2021.12.07)
USP通則(zé)<621>色譜(pǔ)法
